Niels Bohr
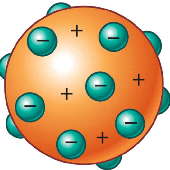
Joseph John Thomson
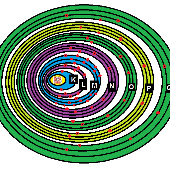
Cada uno de los niveles de energía posee subniveles de energía Estos son: s,p,d,f. Cada uno de ellos aguanta con un número de electrones. Así: El s:2 electrones. El p:6 electrones. El d:10 electrones. El f:14 electrones.
El átomo contenía cargas positivas y negativas
Átomo formado por dos partes: la "corteza" (luego denominada periferia), constituida por todos sus electrones, girando a gran velocidad alrededor de un "núcleo" muy pequeño; que concentra toda la carga eléctrica positiva y casi toda la masa del átomo.
Ernest Rutherford
Actual
John Dalton
Los electrones describen órbitas circulares “NIVELES DE ENERGIA” en torno al núcleo del átomo Les llamo con las letras K L M N O P Q
La materia está formada por partículas muy pequeñas llamadas átomos, que son indivisibles y no se pueden destruir
Joseph John Thomson
John Dalton
Actual
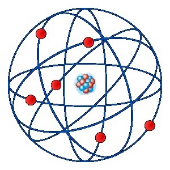


Niels Bohr
Ernest Rutherford