1.
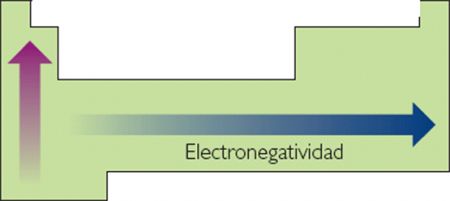
La mayoría de las sustancias que encontramos en la naturaleza están formadas por átomos unidos. Las fuerzas que mantienen unidos a los átomos en las distintas sustancias se denominan enlaces químicos, y se forman de manera tal que al unirse los átomos, adquieran una situación más estable que cuando estaban separados. Por lo cual entonces se obtienen diferentes tipos de enlace, la clasificación de estos enlaces depende de manera general de las propiedades de los elementos que lo conforman, pero en específico de la electronegatividad que es la tendencia que tienen los átomos a atraer hacia sí los electrones en un enlace químico, dándose entonces enlaces covalentes donde se unen elementos de electronegatividades altas, iónicos donde se unen elementos de electronegatividades altas y elementos de electronegatividades bajas, y metálicos donde se unen elementos de electronegatividades bajas.A continuación se presenta la tendencia de electronegatividad de los elementos que conforman la tabla periódica.Una molécula cuyos elementos hagan parte de los grupos I A y VII A en la tabla periódica como el bromuro de potasio (KBr)